Đề thi chuyên hóa vào lớp 10 trường THPT Nguyễn Huệ - Hà Nội
Mời các bạn thí sinh nhất là những bạn có nguyện vọng thi vào lớp 10 chuyên môn Hóa tham khảo đề thi chuyên hóa vào lớp 10 có đáp án trường THPT Nguyễn Huệ - Hà Nội để có thêm tài liệu cho kì thi tuyển sinh vào lớp 10 sắp tới nhé.
|
SỞ GD&DT HÀ NỘI TRƯỜNG THPT CHUYÊN NGUYỄN HUỆ |
KỲ THI VÀO LỚP 10 CHUYÊN Môn: Hóa học (Đề gồm 4 câu 01 trang) Thời gian làm bài: 120 phút (không kể thời gian giao đề) |
Câu 1 (2,0 điểm)
- Viết phương trình phản ứng xảy ra (nếu có) khi:
- Cho mẩu Ba vào dung dịch NaCl
- Cho một mẫu Natri vào dung dịch FeCl3.
- Cho bột Fe vào dung dịch AgNO3 dư.
- Sục khí SO2 vào dung dịch KMnO4 sau đó cho tiếp dung dịch BaCl2 dư vào.
- Trong tự nhiên các nguyên tố Ca, Mg có trong quặng đôlômit: CaCO3.MgCO3. Từ quặng này, hãy trình bày phương pháp điều chế CaCO3, MgCO3 ở dạng riêng biệt tinh khiết?
Câu 2 (2,0 điểm)
- Cho 5 chất khí: CO2, C2H4, C2H2, SO2, CH4 đựng trong 5 bình riêng biệt mất nhãn. Chỉ dùng hai thuốc thử, trình bày phương pháp hóa học phân biệt mỗi bình trên và viết các phương trình phản ứng xảy ra. Các dụng cụ thí nghiệm có đủ.
- Dùng một lượng dung dịch H2SO4 10%, đun nóng để hòa tan vừa đủ 0,4 mol CuO. Sau phản ứng, làm nguội dung dịch. Khối lượng CuSO4.5H2O tách ra khỏi dung dịch là 30 gam. Tính độ tan của CuSO4 trong điều kiện thí nghiệm trên.
Câu 3 (2,0 điểm):
- Có sơ đồ biến đổi sau: X ® Y ® Z ® X ® Q
Biết rằng X là đơn chất của phi kim T còn Y, Z là hợp chất gồm 2 nguyên tố, trong đó có chứa T. Dung dịch chất Y làm quỳ tím hóa đỏ. Z là muối của kali, trong đó kali chiếm 52,35% về khối lượng. Q là hợp chất (gồm ba nguyên tố) tạo thành khi cho X tác dụng với dung dịch xút ở nhiệt độ thường.Xác định CTHH của các chất X, Y, Z, Q và viết PTHH biểu diễn các biến đổi trên.
- Đốt cháy 8,64 gam hỗn hợp Mg và Fe trong khí O2, thu được 12,32 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 12,8 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Tính m?
Câu 4 (2,0 điểm):
- Cho 3 chất hữu cơ đơn chức: axit X (RCOOH); rượu Y (R’OH); este Z tạo bởi axit X và rượu Y (RCOOR’).
- Nếu lấy một lượng hỗn hợp gồm X và Z tác dụng vừa đủ với 150 ml dung dịch NaOH 2M (đun nóng) thì thu được 24,6 gam muối Natri.
- Nếu lấy 13,8 gam Y tác dụng hết với 11,5 gam Natri thì thu được 25 gam bã rắn khan. Xác định công thức cấu tạo của X, Y, Z.
- Ba chất hữu cơ A, B, C chứa cùng nhóm chức có công thức phân tử tương ứng là CH2O2, C2H4O2, C3H4O2.
- Viết công thức cấu tạo và gọi tên các chất A, B, C.
- Tính khối lượng chất B trong dung dịch thu được khi lên men 1 lít rượu etylic 9,20. Biết hiệu suất phản ứng quá trình lên men là 80% và khối lượng riêng của rượu etylic nguyên chất là 0,8g/ml.
Câu 5 (2,0 điểm):
- A là ancol có công thức R(OH)n với R là gốc hidrocacbon. Cho 12,8 gam dung dịch của A trong nước có nồng độ 71,875% tác dụng với Na dư thu được 5,6 lít H2 (đktc). Xác định công thức phân tử và vết công thức cấu tạo của A biết khối lượng phân tử của A là 92.
- Xà phòng hoá hoàn toàn 0,1 mol một este no đơn chức (có công thức CnH2n+1COOCmH2m+1, n, m nguyên, n≥ 0, m ≥1) bằng 28 gam dung dịch MOH 20% (M là kim loại kiềm) rồi tiến hành chưng cất sản phẩm thu được 27 gam chất lỏng X và 9,8 gam chất rắn khan Y. Đốt cháy hoàn toàn chất rắn Y thu được V lít CO2(đktc), H2O và 7,42 gam một muối duy nhất. Tìm công thức của este, tính giá trị của V?
Cho: H=1, C=12, O=16, Na=23, Mg=24, S= 32, Cl=35,5, K=39, Fe=56, Cu=64, Br=80, Ag=108
--------------------------- Hết ---------------------------
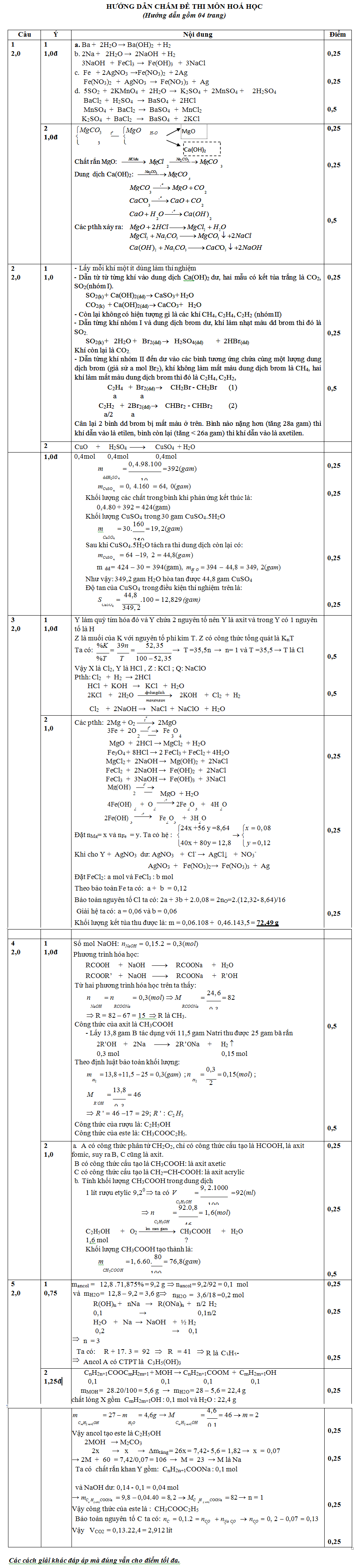
Dưới đây là đáp án đề thi vào lớp 10 chuyên hóa trường THPT Nguyễn Huệ để các bạn có thể tính điểm của mình khi thử sức với đề thi này:
Trong kì thi tuyển sinh tới đây, phụ huynh và học sinh có thể tham khảo thêm các thông tin về điểm chuẩn, tra cứu điểm thi THPT Quốc gia 2017, 2018 tại trang diemthilop10.info nhé. Chúc các thí sinh có một kỳ thi tuyển sinh và có điểm thi vào lớp 10 THPT đạt kết quả cao như mong muốn và luôn đồng hành cùng để biết được kết quả sớm nhất và tiết kiện công sức tìm kiếm và chờ đợi nhé!
Bài viết cùng chuyên mục
-

Kinh nghiệm chọn trường vào lớp 10 thpt cho con hữu ích
-

Tóm tắt quy chế tuyển sinh vào lớp 10 thpt hiện nay
-

Danh sách các trường thpt chuyên năng khiếu toàn quốc
-
Top 100 trường thpt tốt nhất hiện nay
-

Điểm chuẩn vào lớp 10 THPT Công Lập tại Hà Nội năm 2015–2016
-

Danh sách các trường THPT ở Hà Nội chất lượng tốt

